帕金森综合征并不等于帕金森病(PD)。严格来讲,帕金森病应该叫做原发性帕金森病,无明确病因。而帕金森综合征是继发性的,通常由脑外伤、中毒、药物、脑血管病、肿瘤、炎症等原因引起,拳王阿里退役时便被诊断为帕金森综合征。药物是引起帕金森综合征的病因之一。从临床表现看,药源性帕金森综合征(DIP)和PD很相似,非常容易误诊。本文将对DIP的诊断、鉴别诊断、预防和治疗进行阐述。
医脉通编译整理,未经授权请勿转载。
DIP的概述
DIP是PD的第二大病因,发病年龄从10个月到96岁不等,半数患者的年龄在60-79岁之间。其临床表现多样,DIP通常表现为对称性少动-强直综合征(akinetic-rigid syndrome),静止性震颤和冻结步态。回顾既往关于DIP的研究,研究人员得出了以下结论:药物、性别差异都会影响患者的临床表现,DIP的震颤率较PD更高等。比如抗抑郁药、外周多巴胺拮抗剂、中枢多巴胺拮抗剂和第一代抗组胺药物导致的DIP患者最常发生强直,而钙通道阻断剂引起的DIP最常发生震颤。
DIP与PD的鉴别诊断
DIP一直是PD诊断标准中的排除项。DIP的特征和PD很相似,但并非完全一样,通常会导致误诊。DIP病情进展快,同时症状也比较严重,早期可能就会存在平衡障碍、易摔倒、吐字不清等症状。最重要的区别是患者有无吩噻嗪类、丁酰苯类、利舍平、锂剂、α-甲基多巴、甲氧氯普胺、氟桂利等用药史。目前,上述药物的应用相当普遍,应引起重视。遗憾的是,除此之外,目前没有足够的病例数据支持根据患者的运动特征清楚区分DIP和PD,辅助鉴别可参考表1。
表1 DIP与PD的辅助鉴别
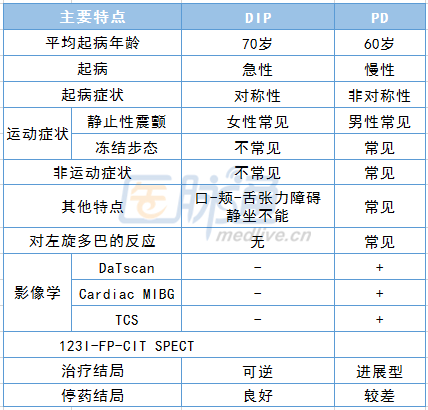
那么,对于长期接受抗精神病药物治疗并逐渐发展为PD的患者,常常会出现这样的疑问:这是真的PD还是DIP?在这些情况下,脑DAT-SPECT显像尤其有效,因为尽管抗精神病药物对大脑多巴胺能系统有显著影响,但这些药物对脑部多巴胺转运体(DAT)的亲和力可忽略不计,不会改变DAT的密度,因此药物对DAT-SPECT的影响可忽略不计。
DIP的治疗经验
DIP患者均有明确的用药史,起病急、进展迅速。确认DIP后,需要了解患者的药物不良反应史,药物引起的帕金森综合征与剂量大小有关,个别患者则可能对此类药物有易感性,应判断责任药物并立即停用,用其他无DIP风险的药物代替。使用新药时,应谨慎并严密观察。如果判断是单纯DIP,可不用抗PD药物,或者试用一段时间后可尝试停药。
多数DIP是可逆的,绝大部分患者在停止服用药物后数周至6个月后帕金森综合征的症状即可明显减轻或消失,无需进行药物治疗。在一项有关DIP的治疗研究中,采取多巴丝肼治疗后部分患者的症状得到缓解,但是部分患者症状未见缓解,治疗效果不佳。且患者在采用多巴丝肼治疗期间,常出现以胃肠道不适为主的不良反应。虽然未发生因不能耐受不良反应而停药的患者,但该研究显示对DIP患者进行药物治疗效果往往不佳。对于不能停药的患者,则应减量。
起初考虑DIP,若停用责任药物后不可逆,可能是药物诱发提前发病的PD(占10%-25%),需抗PD药物并及时调整用药。思考PD的病因分层及SWEDD(scans without evidence of dopaminergic deficit,扫描无多巴胺能缺乏证据)解释。
DIP的预防策略
DIP的治疗和控制较困难,因此预防其发生显得尤为重要。预防策略如下:
(1)使用抗精神病药物通常同时给予抗胆碱能药物,如阿托品、苯海索等,可使药物引起的帕金森综合征减轻或不发生。但若患者对抗胆碱能药物无效,则需要减少抗精神病药物的剂量、停药或改用其它药物。
(2)使用钙通道阻滞剂氟桂利嗪或桂利嗪等药时,疗程不宜过长,剂量宜小,且间歇用药更为合理,用药过程中应密切观察,一旦出现症状应尽早停用。
(3)由胃肠动力药及钙通道阻滞剂而引起的运动或姿势性震颤,必要时可选用苯海索缓解震颤,但老年人使用容易引起尿潴留。
(4)左旋多巴对药源性帕金森综合征的效果不明显,因此不宜作为预防性用药。
(5)注意药物的迟发反应。避免不必要的联合用药,了解患者自用药情况,避免重复用药。
小结
DIP可以在停药、减少剂量或更换副作用更小的药物后得以逆转。临床医生应谨慎选择药物,注重神经系统的保护。只要我们充分认识、了解DIP临床特点,并提高警惕,规范用药,实现早预防、早发现、早治疗的“三早”方针,便可改善患者生活质量,预防并减少DIP。
参考文献:
[1] Emmanuelle Bondon-Guitton, et al. Drug-Induced Parkinsonism: A Review of 17 Years’ Experience in a Regional Pharmacovigilance Center in France[J]. Movement Disorders, 26(12), 2226–2231. doi:10.1002/mds.23828.
[2] Matthias H€ollerhage. Secondary parkinsonism due to drugs, vascular lesions, tumors, trauma, and other insults[J]. International Review of Neurobiology, Volume 149. doi: https://doi.org/10.1016/bs.irn.2019.10.010.
[3] Emmanuelle Bondon, et al. Drug-Induced Parkinsonism: A Review of 17 Years’ Experience in a Regional Pharmacovigilance Center in France Emmanuelle Bondon-Guitton. Movement Disorders:Official Journal of the Movement Disorder Society. Published on 14 Jun 2011, 26(12):2226-2231. doi:10.1002/mds.23828 .
[4] G Ka¨gi, K P Bhatia, E Tolosa. The role of DAT-SPECT in movement disorders[J]. J Neurol Neurosurg Psychiatry 2010;81:5–12. doi:10.1136/jnnp.2008.157370.
[5] 张逊娟. 药源性帕金森综合征患者63例临床症状与治疗分析[J]. 中国卫生产业,2013, 10(36).
[6] 彭兰. 药源性帕金森综合征患者的临床症状与治疗分析[J]. 医学信息2014, (22). doi: 10.3969/j.issn.1006-1959.2014.22.703.
[7] 魏虹, 刘芝修, 李祥, 等. 31例药源性帕金森综合征临床分析[J]. 中医药临床杂志,2010,22(11):972-973.
[8] 张美增, 李鑫, 刘涛,等. 老年神经病学[M]. 北京:科学技术文献出版社. 2017.